近日,复旦大学附属华山医院运动医学科陈世益教授团队,携手中国科学院上海硅酸盐研究所刘宣勇教授、邱家军教授在《细胞》(Cell)杂志子刊《Chem》发表最新研究成果“自组装生物活性水凝胶在大体积肌肉缺损中调控免疫与肌再生的多组学分析”。研究人员开发出一种可注射、自组装的多功能生物活性水凝胶SiCP@InjGel,有望用于严重肌肉缺损的修复。
□通讯员 罗智文 特约记者 刘燕
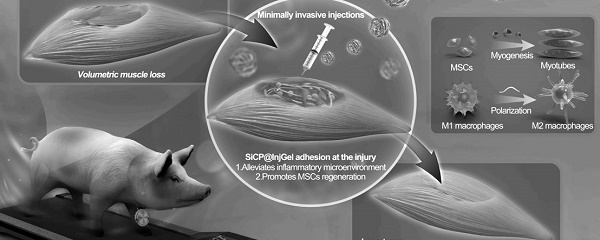
三种天然成分“注射即生肌”
骨骼肌损伤是运动医学领域常见的疾病之一。骨骼肌损伤修复不良可导致肌肉萎缩和功能丧失。许多运动员都曾长期饱受肌肉损伤困扰,对职业生涯造成了严重影响。
容积性肌肉损失是指肌肉损失超过20%的不可恢复性损伤,常由创伤、骨折、肿瘤切除或退行性疾病引发。严重容积性肌肉损失常存在损伤表面不规则、局部免疫微环境紊乱、骨骼肌再生能力受限等问题,且缺乏有效修复手段,导致患者运动功能明显受损,因此被认为是“难题中的难题”。
华山医院运动医学团队在骨骼肌损伤修复方面已经持续深耕二十余年。陈世益教授团队与材料学、免疫学等不同领域科学家交叉合作,尝试了一系列创新策略。此次发表的研究成果针对严重容积性肌肉损失的特点设计了兼具仿生支架、免疫调控和再生促进等多重功能的新型水凝胶材料,为这一临床难题提供了全新的解决思路。
传统肌肉移植治疗和合成材料填补治疗因创伤较大或疗效有限导致临床应用受限。研究人员创新材料设计,利用葛根素、壳聚糖与介孔二氧化硅纳米颗粒三种天然成分制备出新型水凝胶。该水凝胶具备优异的生物相容性与原位成胶特性,注射后能快速凝胶、紧密贴合创面并逐步降解,智能匹配修复进程。
研究人员介绍,葛根素可抑制炎症并诱导M2型巨噬细胞极化;介孔二氧化硅释放的硅离子可促进肌源干细胞增殖分化;壳聚糖提供的三维支架可支持组织重建。三种成分协同作用,可显著促进容积性肌肉损失的修复。
重建肌肉再生闭环
在该研究中,研究人员结合单细胞转录组、质谱流式与蛋白组学等多组学手段,系统揭示了水凝胶的作用机制。
结果显示,这款新型水凝胶可显著增加Pdpn﹢M2型巨噬细胞比例,抑制炎性因子表达,同时激活MyoG﹢肌源干细胞,促进新的肌纤维形成。
组织学与功能学评估表明,该材料通过免疫调控与干细胞激活双向协同,构建起“免疫—干细胞—再生”闭环机制,进而实现损伤肌肉的结构与功能双重建。
有望从实验室走向临床
在小鼠、大鼠及猪等多种动物模型中,这款新型水凝胶均展现出显著的组织再生与功能恢复能力。影像学、超声、组织学及行为学评估一致显示:该材料可促进新生肌肉的功能化重建,并在术后数月内被完全吸收。尤其在猪模型中,使用该材料后,实验动物的步态与抓力可恢复至接近正常水平。
该研究由中国科学院上海硅酸盐研究所、上海交通大学等多学科团队协作完成,体现了“源于临床、服务临床”的科研导向,为严重肌肉损失的微创修复提供了创新性“可注射、可降解、可调控”的再生医学新方案。该研究得到了国家自然科学基金、深圳“三名工程”等支持。
陈世益教授团队长期深耕组织修复、再生医学与运动健康研究,围绕“从材料创新到机制解析,再到临床转化”构建了系统性的科研布局。相关研究成果先后在《自然·纳米技术》《细胞报告》《先进功能材料》《先进复合与杂化材料》《生物活性材料》等国际期刊发表。
在组织修复与再生方向,团队开发出多功能可注射水凝胶和纳米酶材料,系统揭示了“免疫调控—干细胞激活—组织重建”协同机制,为骨骼肌与肌腱再生提供了新策略;在人工韧带创新与临床转化方面,团队构建出分级螺旋碳纳米管人工韧带,实现了优异的骨整合与功能重建,研究成果入选《中国2023年度重要医学进展》;在运动促进健康机制研究中,团队揭示运动改善阿尔茨海默病的新机制,为精准运动干预提供了科学依据。相关研究成果为未来精准干预与功能重建的临床应用奠定了坚实基础,并为再生医学与运动健康领域的发展注入了新活力。